近日,我校衡阳医学院肿瘤研究所杨晴来团队教授在国际权威期刊《Theranostics》(中科院一区,IF:11.6)发表了题为“Clearance pathways of near-infrared-II contrast agents”的长篇综述论文,南华大学衡阳医学院为第一单位,肿瘤研究所2020级博士生杨沙为第一作者,杨晴来教授、谭啸峰教授和唐立教授为共同通讯作者。
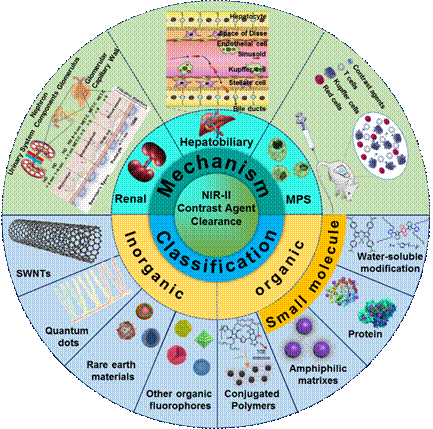
近红外二区(NIR-II)生物成像技术正逐渐发展成为生物医学研究的一项重要可视化检测工具。具备良好光学性能和生物相容性的造影剂是NIR-II成像技术在医学研究领域中发挥优势作用的关键因素。然而,大多数NIR-II造影剂在体内器官滞留引起的生物毒性限制了其临床转化。因此,掌握NIR-II造影剂的药代动力学特性,优化其体内清除途径,减少脏器滞留以降低长期毒性显得尤为重要。
造影剂的清除在体内主要经过单核-巨噬细胞系统(MPS)、肝胆和肾脏三大清除途径,其清除与血液循环和吞噬细胞降解特性直接或间接相关。简而言之,造影剂的清除途径取决于多种综合因素,主要包括造影剂的成分、大小、形状、电荷和表面修饰。小的动力学直径(HD) (< 6 nm)或低分子质量(MW) (< 40 kDa)的造影剂可有效通过肾脏清除。相比之下,大尺寸或高分子质量的材料(>8 nm或40 kDa)主要被单核-巨噬细胞系统(MPS)和肝胆途径清除。值得注意的是,一些大分子的造影剂也可在体内降解后经血液循环被肾脏清除。一般来说,表面为中性或微负电荷的造影剂是有益于在体内进行长时间循环。相反,带正电荷的造影剂更易于被吞噬细胞摄取,缩短其在血液循环的半衰期。此外,对造影剂进行亲水性聚合物(例如,PEG)的修饰可有效降低MPS的摄取。就形状而言,棒状造影剂有利于避免血清蛋白附着,降低MPS的摄取。然而,无法清除的造影剂在体内的生物积累会导致不可预知的慢性毒性。
本文综述了生物材料的清除机制,包括MPS、肾脏和肝胆清除机制。重点对NIR-II造影剂包括无机、有机和其他复合材料的清除途径进行了详细阐述。此外,根据造影剂的结构特点,系统分析了各种造影剂的清除机制,为进一步开发具有可清除特性和良好生物相容性的NIR-II造影剂提供了有力的理论依据。
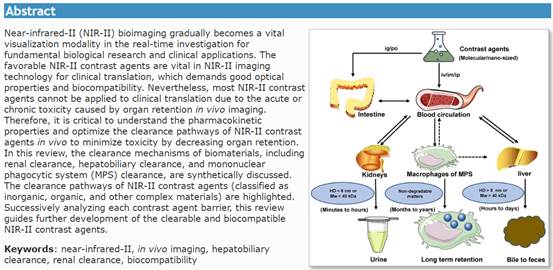
肾脏清除途径具有快速排泄特性,可有效缓解外源性造影剂在体内的生物学毒性,明显优于肝胆清除和MPS清除途径,因此,肾脏清除是NIR-II造影剂的首选途径。为了将NIR-II造影剂的应用从目前的临床前阶段扩展到临床诊疗的可转化阶段,在此提出了一些建议和展望:①具有肾脏清除特点的传统的Vis-NIR造影剂可作为NIR-II造影剂研发的参考。合理的结构工程策略和表面修饰有助于减少NIR-II造影剂在内脏和生物组织的滞留,有效促进肾脏清除。②精准工程策略是精确调控NIR-II造影剂清除特性的有效途径。比如,采用物理包埋法制备的纳米NIR-II造影剂策略可有效增加造影剂在肿瘤部位的积累,并能有效延长滞留时间。③从另一个角度来看,开发可清除的NIR-II造影剂可实现良好的生物安全性。另外,不同的给药形式(如口服、吸入、喷雾涂层)也可一定程度解决现有NIR-II造影剂的在体内的长期毒性问题。④从生物来源的物质中获得具有生物相容性NIR-II造影剂是突破生物安全性的捷径,遵循“取之于自然,用之于自然”的规则,可有效避免外源性、合成的NIR-II造影剂所面临的清除障碍。
杨晴来教授团队长期致力于NIR-II生物材料的诊疗研究,已在Advanced Materials,2017;PNAS,2017;Journal of the American Chemical Society,2018, ;Angew. Chemie,2020; Small,2020;ACS Appl Mater Interfaces,2022;Journal of Nanobiotechnology,2022等国际学术期刊发表多项研究成果。
论文链接:https://www.thno.org/v12p7853.htm


